Ilmuan AS Temukan Karakteristik Antibodi Terapeutik Untuk Cegah Infeksi Virus Corona
Sebuah tim peneliti dari A-Alpha Bio Amerika Serikat, saat ini melakukan proses Screening besar-besaran terhadap 33 Antibodi Terapeutik,
untuk memeriksa sejumlah afinitas pengikatnya terhadap sejumlah varian Coronavirus 2 (SARS-CoV-2), sindrom pernafasan akut yang masuk kategori kritis atau parah.
Tim ini menganalisis dampak mutasi potensial pada puncak receptor-binding Domain (RBD) pada kemanjuran antibodi.
Baca Juga :
Ilmuwan Jepang Berhasil Temukan Formula Energi Surya Ramah Lingkungan
Hasil studi ini dipublikasikan dan sudah tersedia saat ini di server bioRxiv.
Karakterisasi Afinitas Terapeutik yang Digandakan Secara Massal Terhadap Varian SARS-CoV-2. Sumber : Design_Cells / Shuttershock
Latar Belakang Studi
Antibodi monoklonal terapeutik yang dikembangkan untuk melawan SARS-CoV-2 terbukti manjur dalam mengurangi parahnya dan kematian penyakit akibat virus Corona (Covid 19) baik dalam uji klinis maupun situasi pandemi didunia nyata.
Beberapa kandidat antibodi saat ini sedang menjalani uji klinis fase 2 dan 3, dengan beberapa diantaranya sudah menerima persetujuan penggunaan darurat dari otoritas kesehatan diseluruh dunia.
Awalnya dicoba ke hewan, dan kini sudah masuk ke tahap uji coba pada manusia.
Sebagian besar Antibodi Terapeutik ini dirancang untuk menargetkan RBD SARS-CoV-2 yang merupakan evolusi dari virus Covid 19.
Interaksi antara RBD, dan enzim pengubah angiotensin sel inang 2 (ACE2) dapat terganggu.
Oleh karena itu, terbukti bahwa mutasi yang timbul pada lonjakan RBD berpotensi mengubah efektivitas pengikatan RBD dari antibodi.
Dalam konteks ini, penelitian telah menunjukkan bahwa varian SARS-CoV-2 yang baru muncul dengan mutasi RBD spike mampu lolos dari netralisasi yang dimediasi antibodi.
Hasil Studi Antibodi Terapeutik
Dalam studi saat ini, para ilmuwan telah memeriksa afinitas pengikatan dari 33 kandidat antibodi terapeutik untuk panel besar varian SARS-CoV-2.
Di antara antibodi yang diuji, terdapat 9 antibodi yang relevan secara klinis, termasuk Imdevimab, Casirivimab, Etesevimab, dan Bamlanivimab.
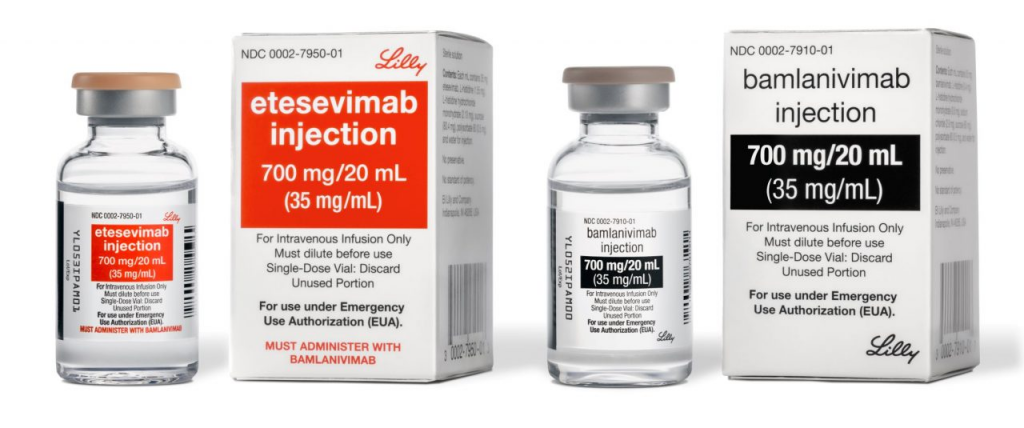
Vaksin Antibodi jenis bamlanivimab, dan Etesevimab. Foto : www.pharmaceutical-technology.com
Dengan menggunakan uji AlphaSeq, mereka telah menilai lebih dari 150.000 interaksi protein-protein antara antibodi dan sebagian besar mutasi substitusi asam amino tunggal yang ada pada lonjakan RBD.
Dalam analisis, mereka juga memasukkan sejumlah varian SARS-CoV-2 yang beredar dengan banyak lonjakan mutasi.
Selain itu, mereka telah menganalisis interaksi protein-protein untuk mengidentifikasi epitop utama untuk setiap antibodi,
serta untuk mendeteksi mutasi yang bertanggung jawab atas hilangnya kemampuan pengikatan epitop dari setiap antibodi.
Dengan secara khusus menganalisis efisiensi ke-9 antibodi yang relevan secara klinis,
para ilmuwan mengamati tidak ada variasi yang signifikan dalam afinitas pengikatan Imdevimab, Casirivimab atau Bamlanivimab untuk varian B.1.1.7.
Namun, mereka mendeteksi penurunan afinitas pengikatan Casirivimab dan Bamlanivimab untuk varian B.1.351 dan P.1.
Penurunan serupa dalam afinitas pengikatan yang mereka amati untuk Regdanvimab dan COR-101 dan Tixagevimab ke varian B.1.1.7, B.1.351, dan P.1 dan varian B.1.351, dan P.1.
Mengenai reaktivitas silang, mereka mengamati bahwa sementara Imdevimab, Bamlanivimab, Regdanvimab, Tixagevimab, Cilgavimab, dan COR-101 sangat spesifik
untuk RBD lonjakan SARS-CoV-2, Casirivimab, Sotrovimab, dan Etesevimab menunjukkan tingkat reaktivitas silang yang berbeda RBD dari virus korona terkait, seperti SARS-CoV-1, LYRa11, WIV1, dan RaTG13.
Penelitian ini juga mengkarakterisasi afinitas pengikatan antibodi yang relevan secara klinis untuk varian baru atau evolusi dari virus Covid, menyoroti dampak mutasi RBD pada kemanjuran antibodi.